Автор Закари Стибер через The Epoch Times (выделено нами),
Moderna собирается попросить регулирующие органы одобрить ее комбинированную вакцину против COVID-19 и гриппа компания сообщила 30 июня.
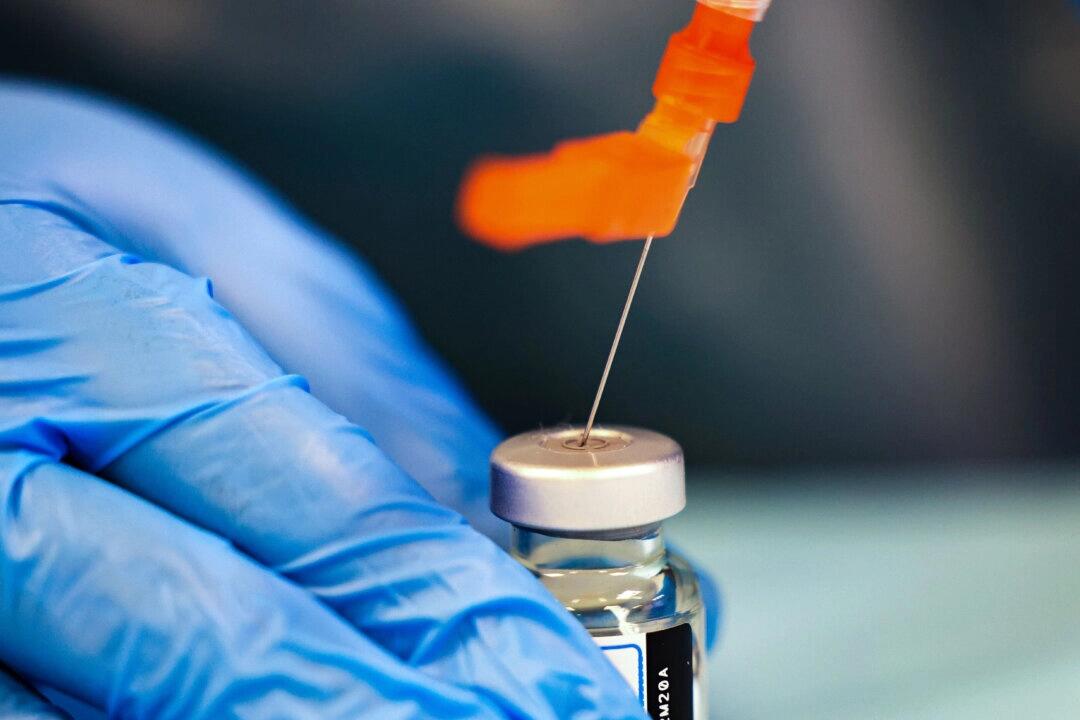
Компания заявила, что исследование фазы 3, оценивающее ее вакцину-кандидат против гриппа мРНК-1010 —в которой используется та же платформа информационной рибонуклеиновой кислоты (мРНК), что и ее вакцина против COVID-19—, показало положительную эффективность.
В исследовании, в котором приняли участие 40 805 человек и сравнивали мРНК-1010 с существующей вакциной против сезонного гриппа у взрослых в возрасте 50 лет и старше, относительная защита от кандидата была на 26,6 процента лучше. При анализе подгрупп среди участников в возрасте не менее 65 лет относительная эффективность составила 27,4 процента.
“Сегодняшние высокие результаты эффективности фазы 3 являются важной вехой в наших усилиях по снижению бремени гриппа у пожилых людей,” Стефан Бансель, генеральный директор Moderna, сказал в заявлении.
Несколько компаний, включая Moderna, планируют внедрить комбинированные прививки от COVID-19 и гриппа.
Однако Moderna в мае снято его заявка на одобрение комбинированной вакцины, по словам компании, этот шаг был предпринят после консультации с Управлением по контролю за продуктами и лекарствами.
В то время компания Moderna заявила, что планирует повторно подать заявку до конца 2025 года после получения данных об эффективности третьей фазы исследования мРНК 1010.
“Вакцина против гриппа на основе мРНК имеет потенциальное преимущество, позволяющее более точно сопоставлять циркулирующие штаммы, поддерживать быстрое реагирование на будущую пандемию гриппа и прокладывать путь для комбинированных вакцин против COVID-19, - заявил Бансель в понедельник.
Результаты испытаний были полностью опубликованы или рецензированы. Moderna заявила, что планирует представить результаты в рецензируемый журнал.
Moderna заявила, что результаты рандомизированного исследования фазы 3 показали результаты безопасности, аналогичные тем, которые были получены сообщаемый из другого исследования фазы 3, опубликованного в марте в журнале Vaccine. В этой статье исследователи сообщили о одинаковом количестве нежелательных явлений у реципиентов вакцины Moderna и добровольцев, получивших существующие вакцины против гриппа. Среди реципиентов Moderna также было меньше тяжелых, серьезных и медицинских нежелательных явлений, при этом в этой группе не было зарегистрировано ни одного случая смерти.
“Большинство предполагаемых побочных реакций (ПРР) были легкими”, — говорится в заявлении Moderna о новом исследовании. “Боль в месте инъекции была наиболее распространенным местным САР, а усталость, головная боль и миалгия были наиболее распространенными системными САР.
“Между группами не было существенных различий в частоте нежелательных нежелательных явлений, серьезных нежелательных явлений или нежелательных явлений, представляющих особый интерес.”
В настоящее время в США нет мРНК-вакцин против гриппа.
FDA не ответило на запрос о комментарии к моменту публикации.
Регуляторы в мае одобрено новая вакцина от COVID-19 от Moderna для взрослых в возрасте 65 лет и старше, а также других лиц в возрасте не менее 12 лет, у которых есть одно или несколько заболеваний, о которых говорят официальные лица поставь их с более высоким риском тяжелой формы COVID-19.

Комментариев нет:
Отправить комментарий