Как «развернуть» спайковый белок C81
Рецензируемое медицинское исследование показывает, что две распространенные добавки, отпускаемые без рецепта, объединяются для уничтожения шиповидного белка SARS-CoV-2. В этой статье перепечатано рецензируемое исследование и рассказывается, какие ОНИ использовали добавки, которые уничтожили спайковый белок. Может быть, люди, принявшие «вакцины», могут использовать это, чтобы уничтожить в себе спайковые белки, от которых многие из них заболевают, а многих убивают?
В интересах полного раскрытия информации я НЕ продаю какие-либо добавки, упомянутые здесь, и НЕ ЗАРАБАТЫВАЮ ДЕНЕГ ни от кого за передачу этой информации вам. Я делаю это как государственную услугу.
Эта рецензируемая статья была опубликована в марте 2021 года, но никто в СМИ не удосужился сообщить об этом общественности. Единственное, что сделали СМИ, это протолкнули «воск». Теперь многие люди мертвы, умирают или очень больны от прививки.
Похоже, что информационная РНК в ваксе заставляет наши человеческие клетки «экспрессировать шиповидный белок», подобный тому, который присутствует в коронавирусе, вызывающем COVID. За исключением того, что человеческие клетки не __предположительно__ "экспрессируют спайковый белок".
Ниже приведено исследование, которое показало, что две безрецептурные пищевые добавки, бромелайн и ацетилцистеин (NAC), при совместном использовании, а не по отдельности , вызывают разрушение белковых связей и их растворение. Изображения результатов ниже!
Комбинация бромелаина и ацетилцистеина (BromAc) синергетически инактивирует SARS-CoV-2
- Вступление
Недавно появившийся коронавирус тяжелого острого респираторного синдрома 2 (SARS-CoV-2) является возбудителем коронавирусной болезни 2019 (COVID-19), которая может варьироваться от бессимптомных до тяжелых и летальных форм с синдромом системной воспалительной реакции. По состоянию на 21 февраля 2021 г. было зарегистрировано более 111 миллионов подтвержденных случаев с расчетной общей смертностью в 2,2% [ 1 ]. В настоящее время существует несколько терапевтических агентов, которые доказали свою эффективность в снижении прогрессирования заболевания на ранних и поздних стадиях [ 2 ]. Хотя, к счастью, существует много вакцин-кандидатов, их широкое распространение для вакцинации может произойти не сразу, а продолжительность иммунной защиты может быть ограничена [ 3 , 4 ].], а эффективность вакцин может быть снижена новыми вариантами SARS-CoV-2. Поэтому по-прежнему необходимо продолжать изучение эффективных методов лечения.
Структурно SARS-CoV-2 содержит поверхностные шиповидные белки, мембранные белки и белки оболочки, а также внутренние нуклеопротеины, которые упаковывают РНК. Спайковый белок представляет собой гомотримерный гликопротеиновый комплекс с различными ролями, выполняемыми за счет динамических конформационных модификаций, частично основанных на дисульфидных связях [ 5 ]. Он позволяет инфицировать клетки-мишени путем связывания с рецепторами человеческого ангиотензинпревращающего фермента (ACE2), среди прочего, что запускает протеолиз трансмембранной протеазой серином 2 (TMPRSS2), фурином и, возможно, другими протеазами, что приводит к образованию вириона и мембраны клетки-хозяина. слияние [ 6 , 7 ].
Проникновение вирусов в клетки млекопитающих, или «интернализация вируса», является ключевым механизмом оболочечной вирусной инфекции и основано на динамических конформационных изменениях их поверхностных гликопротеинов, а именно опосредованных восстановлением дисульфидных связей и регулируемых оксидоредуктазами и протеазами клеточной поверхности. [ 5 , 8 , 9 , 10 , 11 ]. Было показано, что проникновение SARS-CoV-2 в клетки-хозяева начинается с дестабилизации шиповидного белка посредством аллостерического механического перехода, который вызывает конформационное изменение из закрытого «нижнего» состояния в открытое «верхнее» состояние домена связывания рецептора (RBD). ) шиповидного белка [ 12 , 13]. Конформационные изменения RBD и связывание вируса индуцируются TMPRSS2 или катепсином L, которые запускают переход от состояния до слияния к состоянию после слияния [ 5 , 12 , 13 ]. Энергия, высвобождаемая при восстановлении дисульфидных связей, увеличивает гибкость белка, которая максимальна, когда восстановленное состояние завершено [ 8 ], что позволяет осуществить слияние мембран вируса-хозяина, что в противном случае невозможно из-за отталкивающих сил гидратации, присутствующих до восстановления [ 5 ] . .
Бромелайн извлекается в основном из стебля ананаса ( Ananas comosus ) и содержит ряд ферментов, которые придают ему способность гидролизовать гликозидные связи в сложных углеводах [ 14 ]. Предыдущие исследования показали, что бромелайн удаляет спайки и белки гемагглютинина вируса Леса Семлики, вируса Синдбиса, желудочно-кишечного коронавируса мышей, вируса гемагглютинирующего энцефаломиелита и вирусов гриппа H1N1 [ 15 , 16 ].]. В качестве терапевтической молекулы он используется для обработки ожогов. Ацетилцистеин является мощным антиоксидантом, который обычно распыляют в дыхательные пути для скопления слизи, а также используют в качестве гепатопротекторного средства при передозировке парацетамола. Наиболее важно в данном контексте то, что ацетилцистеин уменьшает дисульфидные связи [ 17 ]. Более того, ассоциация белков шипа и оболочки их соответствующими тройными цистеиновыми мотивами подтверждает гипотезу о воздействии на стабильность вириона после разрушения дисульфидного мостика под действием ацетилцистеина [ 18 ]. Комбинация бромелаина и ацетилцистеина (BromAc) проявляет синергический муколитический эффект, который используется при лечении муцинозных опухолей [ 19 , 20 ].] и в качестве химиосенсибилизатора нескольких противоопухолевых препаратов [ 21 ]. Эти различные действия обусловлены способностью BromAc разворачивать молекулярные структуры сложных гликопротеинов, что позволяет происходить связыванию из-за высокого сродства между RBD и ACE2.
Поэтому в текущем исследовании мы намеревались определить, может ли BromAc нарушать целостность белков шипа и оболочки SARS-CoV-2, а затем изучить его потенциал инактивации в отношении репликации in vitro двух вирусных штаммов, включая один с мутантным изменением шипа SARS-CoV-2. новый сайт расщепления S1/S2.
- Материалы и методы
2.1. Материалы
Бромелайн API был изготовлен компанией Mucpharm Pty Ltd (Когара, Австралия) в виде стерильного порошка. Ацетилцистеин был приобретен у Link Pharma (Cat# AUST R 170803; Warriewood, Австралия). Рекомбинантный спайковый белок SARS-COV-2 был получен от SinoBiological (кат. № 40589-V08B1; Пекин, Китай). Рекомбинантный белок оболочки был получен от MyBioSource (кат. № MBS8309649; Сан-Диего, Калифорния, США). Все остальные реагенты были получены от Sigma Aldrich (Сент-Луис, Миссури, США).
2.2. Рекомбинантный гель-электрофорез с шипами и оболочками
Белки шипа или оболочки восстанавливали в стерильной дистиллированной воде в соответствии с инструкциями производителя, а аликвоты замораживали при -20°C. Два с половиной микрограмма белка шипа или оболочки инкубировали с 50 или 100 мкг/мл бромелаина, 20 мг/мл ацетилцистеина или их комбинацией в воде Milli-Q. Контроль не содержал наркотиков. Общий объем реакционной смеси составлял 15 мкл каждой. После 30-минутной инкубации при 37 °C в каждую реакцию добавляли 5 мкл буфера для образцов. В общей сложности 20 мкл каждой реакции подвергали электрофорезу на SDS-PAGE (кат. № 456-1095; Bio-Rad Hercules, Калифорния, США). Гели окрашивали кумасси синим.
2.3. УФ-спектральное обнаружение дисульфидных связей в шиповидных и оболочечных белках
Метод Айера и Клее для измерения скорости восстановления дисульфидных связей был использован для обнаружения дисульфидных связей в шиповидных и оболочечных белках [ 22 ].]. Рекомбинантный шиповидный белок SARS-CoV-2 в концентрации 3,0 мкг/мл в фосфатно-солевом буфере (PBS) (рН 7,0), содержащем 1 мМ этилендиаминтетрауксусной кислоты (ЭДТА), инкубировали с 0, 10, 20, 40 и 50 мкл ацетилцистеина (0,5 М), перемешивали при 37 ° C в течение 30 минут с последующим эквивалентным добавлением дитиотреитола (DTT) (0,5 М) и перемешивали еще 30 минут при 37 ° C. Белок шипа инкубировали параллельно только с DTT (0,5 М), как и раньше, без какого-либо ацетилцистеина и перемешивали при 37°С в течение 30 мин. Затем считывали поглощение при 310 нм. УФ-спектральное обнаружение дисульфидных связей в оболочечном белке проводили аналогичным образом.
2.4. Инактивация всего вируса SARS-CoV-2 с помощью BromAc
В полном соответствии с временными рекомендациями Всемирной организации здравоохранения (ВОЗ) по биобезопасности в отношении коронавирусной болезни тесты на инактивацию цельного вируса SARS-CoV-2 были проведены с использованием штамма дикого типа (WT), репрезентативного для ранних циркулирующих европейских вирусов (инвентарный номер GISAID). EPI_ISL_578176). Второй штамм SARS-CoV-2 (обозначенный как ∆S), зарегистрированный в ходе обычного геномного наблюдения в регионе Овернь-Рона-Альпы во Франции, был добавлен к тестам на инактивацию из-за редкой мутации в месте расщепления шипа S1/S2. и доступность его культуры в лаборатории (инвентарный номер GISAID EPI_ISL_578177).
Эти тесты проводились с возрастающими концентрациями одного бромелаина (0, 25, 50, 100 и 250 мкг/мл), только ацетилцистеина (20 мг/мл) и перекрестной реакцией различных концентраций бромелаина в сочетании с постоянным 20 мг/мл препарата ацетилцистеина против двух разведений вирусной культуры при 10 5,5 и 10 4,5 TCID50/мл. После 1 ч воздействия лекарственного средства при 37 °C все условия, включая контроль, разбавляли в 100 раз, чтобы избежать цитотоксичности, инокулировали в четырех повторностях на конфлюэнтных клетках Vero (CCL-81; ATCC©, Манассас, Вирджиния, США) и инкубировали в течение 5 дней при 36 °C с 5% CO 2. Клетки поддерживали в минимальной основной среде Игла (EMEM) с 2% пенициллином-стрептомицином, 1% L-глютамином и 2% инактивированной эмбриональной бычьей сыворотки. Результаты были получены с помощью ежедневных наблюдений с помощью оптической микроскопии, анализа окрашивания конечного лизиса клеток и полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР) экстрактов супернатантов РНК. Вкратце, анализ окрашивания лизиса клеток в конечной точке состоял из добавления нейтрального красного красителя (Merck KGaA, Дармштадт, Германия) к клеточным монослоям, инкубации при 37 °C в течение 45 минут, промывания PBS и добавления цитрата этанола до оптической плотности (OD). ) измеряли при 540 нм (Labsystems Multiskan Ascent Reader, Thermo Fisher Scientific, Уолтем, Массачусетс, США). ОП была прямо пропорциональна количеству жизнеспособных клеток, поэтому низкая ОП свидетельствует о значительном лизисе клеток из-за репликации вируса. Кроме того,® (bioMérieux, Lyon, FR) и RdRp Institute Pasteur, нацеленный на SARS-CoV-2 IP2, RT-PCR проводили на системе QuantStudio™ 5 (Applied Biosystems, Thermo Fisher Scientific, Фостер-Сити, Калифорния, США). Значения снижения log 10 (LRV) репликации вируса рассчитывали по разнице между лунками с лечебной и контрольной лунками на условие, деленной на 3,3 (поскольку 1 log 10 ≈ 3,3 порога цикла ПЦР (Ct)).
2.5. Кинетика репликации с помощью анализа клеток в реальном времени
Чтобы сравнить репликационную способность in vitro штаммов WT и ∆S SARS-CoV-2, кинетику репликации определяли путем измерения импеданса электродов микроэлектронных клеточных сенсоров на приборе xCELLigence Real-Time Cell Analyzer (RTCA) DP (ACEA Biosciences, Inc., Сан-Диего, Калифорния, США). Клетки Vero высевали по 20 000 клеток на лунку на E-Plate 16 (ACEA Biosciences, Inc., Сан-Диего, Калифорния, США) и инкубировали в тех же условиях среды, что и описанные ранее, при 36 °C с 5% CO2. Через 24 часа культуральные изоляты SARS-CoV-2 инокулировали в трех повторностях при множественности заражения 10–2. Мнимые инфекции были выполнены в четырех экземплярах. Данные электронного импеданса (клеточный индекс) непрерывно собирали с 15-минутными интервалами в течение 6 дней. Площадь под кривой анализа нормализованного клеточного индекса, установленного во время инокуляции, Затем рассчитывали с 12-часовыми интервалами. В каждом интервале жизнеспособность клеток определяли путем нормализации относительно соответствующего клеточного контроля. Для сравнения каждого состояния на GraphPad Prism (версия программного обеспечения 9.0; Сан-Диего, Калифорния, США) использовались множественные сравнительные тесты Тьюки.
- Результаты
3.1. Изменение белков шипа и оболочки SARS-CoV-2
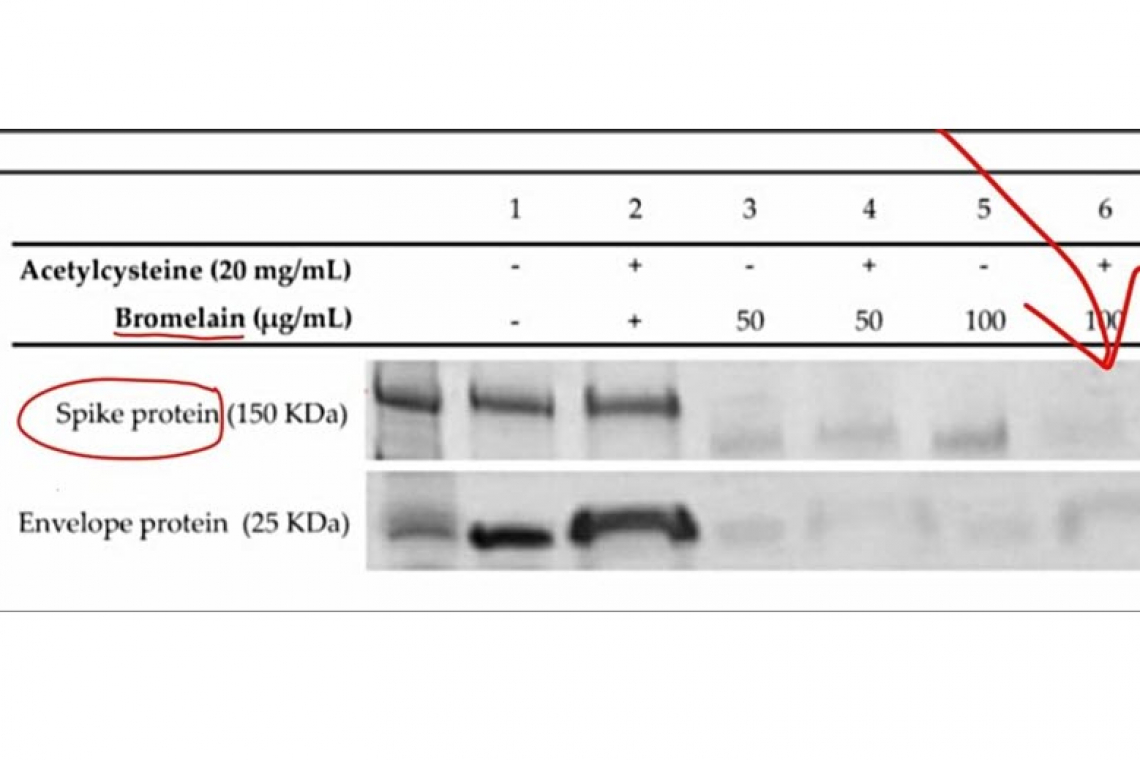
Обработка шиповидного белка только ацетилцистеином не показала каких-либо изменений белка, тогда как концентрации бромелаина в 50 и 100 мкг/мл и BromAc в 50 и 100 мкг/20 мг/мл привели к изменению белка ( рис . 1А ). Обработка ацетилцистеином белка оболочки не изменила белок, тогда как обработка бромелаином в дозах 50 и 100 мкг/мл и BromAc в дозах 50 и 100 мкг/20 мг/мл также приводила к почти полной и полной фрагментации соответственно ( рис . 1А). ).
Рисунок 1. ( A ) Бромелайн и ацетилцистеин оказывают синергетическое действие на спайки коронавируса тяжелого острого респираторного синдрома (SARS-CoV-2) и дестабилизацию белка оболочки. SDS-PAGE субъединиц S1 + S2 рекомбинантного шиповидного белка SARS-CoV-2 (150 кДа) и оболочечного белка (25 кДа). Белки обрабатывали только 20 мг/мл ацетилцистеина, 100 и 50 мкг/мл только бромелаина и комбинацией 100 и 50 мкг/20 мг/мл BromAc. ( Б) Дисульфидное восстановление рекомбинантного спайкового белка SARS-CoV-2 с помощью ацетилцистеина. Дифференциальный анализ между ацетилцистеином (Ас) и дитиотреитолом (ДТТ) на восстановление дисульфидных связей, обнаруженных в шиповидном белке, показывает, что ацетилцистеин уменьшает 42% дисульфидных связей до добавления ДТТ. Оставшиеся связи восстанавливаются с помощью DTT с образованием хромогена, обнаруживаемого при 310 нм. ( C ) Восстановление дисульфида рекомбинантного белка оболочки SARS-CoV-2 ацетилцистеином. Дифференциальный анализ между ацетилцистеином (Ас) и дитиотреитолом (ДТТ) на восстановление дисульфидных связей, обнаруженных на оболочечном белке, показывает, что ацетилцистеин уменьшает 40% связей перед добавлением ДТТ.
3.2. УФ-спектральное обнаружение демонстрирует изменение дисульфидных связей в шиповидных и оболочечных белках
Сравнительное снижение дисульфидных связей на шиповидном белке между одним ДТТ и ДТТ с ацетилцистеином продемонстрировало разницу в 42% ( рис . 1В), исходя из наклона графиков [0,002599/0,006171 (100) = 42 %]. Таким образом, ацетилцистеин смог восстановить 58% дисульфидных связей в образце, после чего оставшиеся дисульфидные связи были восстановлены с помощью DTT с образованием хромогена, который отслеживался в спектрах. Точно так же дифференциальный анализ между ацетилцистеином и ДТТ для восстановления дисульфидных связей, обнаруженных в оболочечном белке [0,007866/0,01293 (100) = 60%], показывает, что ацетилцистеин восстанавливает 40% дисульфидных связей до добавления ДТТ ( рис . 1С ). ).
3.3. Инактивирующий потенциал бромелаина, ацетилцистеина и BromAc в отношении SARS-CoV-2 in vitro
Для обоих испытанных штаммов SARS-CoV-2 необработанные контрольные вирусы при 10 5,5 и 10 4,5 TCID 50 /мл давали типичные цитопатические эффекты (CPE), и никакой цитотоксичности не наблюдалось ни для одной из комбинаций препаратов на клетках Vero. Результаты оптического CPE неизменно подтверждались окрашиванием нейтральных эритроцитов в конечной точке. В целом, обработка бромелаином и ацетилцистеином по отдельности не показала ингибирования вируса, все с CPE, сравнимым с лунками с контролем вируса, тогда как комбинации BromAc показали инактивацию вируса в зависимости от концентрации ( рис. 2 ). Обработка 10 титров вируса 4,5 TCID 50 /мл ( рис. 2 B, D) приводила к более последовательному ингибированию CPE для четырех повторов, чем при 105.5 Титры вируса TCID 50 /мл ( рис. 2 A, C).
Рисунок 2. Анализы лизиса клеток продемонстрировали потенциал инактивации in vitro комбинации ацетилцистеина и бромелаина (BromAc) против SARS-CoV-2. Жизнеспособность клеток измеряли путем окрашивания клеток нейтральным красным, где оптическая плотность (OD) прямо пропорциональна количеству жизнеспособных клеток. Низкая OD будет означать значительный лизис клеток из-за репликации вируса. Штамм SARS-CoV-2 дикого типа (WT) с титрами 5,5 и 4,5 log 10 TCID 50 /мл ( A и B, соответственно) не показали ингибирования цитопатического эффекта (CPE) при лечении одним агентом по сравнению с контрольным состоянием вируса при имитации лечения. Комбинации BromAc были способны ингибировать CPE по сравнению с контрольными клетками с псевдоинфекционными клетками. Лечение варианта шиповидного белка SARS-CoV-2 (∆S) с мутацией на стыке S1/S2 при титрах 5,5 и 4,5 log 10 TCID 50 /мл ( C и D соответственно) показало аналогичные результаты. Столбцы представляют собой среднее значение каждого четырехкратного повторения для каждого условия, показанного белыми кружками. Выполняли обычный однофакторный ANOVA, используя в качестве контрольного условия имитацию вирусного контроля (**** p < 0,0001, *** p < 0,0005, ** p < 0,003 и * p < 0,05).
В соответствии с руководящими принципами инактивации вирусов, установленными ВОЗ, надежный и надежный процесс инактивации сможет снизить репликацию как минимум на 4 log [значение снижения Log 10 (LRV) = (обработка RT-PCR Ct — контроль RT-PCR Ct )/3,3; как 1 log 10 ≈ 3,3 Ct]. Таким образом, ОТ-ПЦР проводили на экстрактах РНК для непосредственного измерения репликации вируса. Для штамма дикого типа (WT) при 10 4,5 TCID 50 /мл успешная LRV> 4 наблюдалась с 1 из 4 лунок, 2 из 4 лунок, 3 из 4 лунок и 4 из 4 лунок в течение 25 дней. , 50, 100 и 250 мкг/20 мг/мл BromAc соответственно ( рис. 3 ). Стоит отметить, что при 10 5,5 TCID 50/мл, LRV был немного ниже порогового значения, в среднем 3,3, с 3 из 4 лунок и 2 из 4 лунок для 100 и 250 мкг/20 мг/мл BromAc соответственно ( таблица 1 ). Для мутанта шиповидного белка (∆S) при 10 4,5 TCID 50 /мл успешная LRV > 4 не наблюдалась для 25 мкг/20 мг/мл BromAc, но наблюдалась в 4 из 4 лунок для 50, 100 и 250 мкг/20 мг/мл BromAc ( рис. 3 ). Следует отметить, что при 10 5,5 TCID 50 /мл LRV была немного ниже порога, в среднем 3,2, с 1 из 4 лунок, 2 из 4 лунок и 4 из 4 лунок для 50, 100 и 250 мкг/20 мг/мл BromAc соответственно ( Таблица 1). В целом инактивация репликационной способности обоих штаммов SARS-CoV-2 in vitro наблюдалась дозозависимым образом, что наиболее ярко проявлялось при 100 и 250 мкг/20 мг/мл BromAc против 10 4,5 TCID 50 /мл вируса.
Рисунок 3. Пороговая матрица значений log 10 снижения (LRV) репликации вируса in vitro через 96 ч после обработки BromAc на штаммах WT и ∆S SARS-CoV-2 при титрах 5,5 и 4,5 log 10 TCID 50 /мл. LRV рассчитывали по следующей формуле: LRV = (RT-PCR Ct лечения - RT-PCR Ct вирусный контроль)/3,3; как 1 log10 ≈ 3,3 Ct. Матрица цветового градиента отображает количество четырехкратных повторов на одно условие, дающее LRV> 4, что соответствует надежной инактивации согласно ВОЗ. WT = дикий тип; ∆S = шиповидный мутант S1/S2.
Таблица 1. Значения снижения log 10 (LRV) репликации вируса in vitro через 96 ч после обработки BromAc на штаммах WT и ∆S SARS-CoV-2 при титрах 5,5 и 4,5 log 10 TCID 50 /мл. LRV рассчитывали по следующей формуле: LRV = (RT-PCR Ct лечения – RT-PCR Ct вирусный контроль)/3,3; как 1 log 10 ≈ 3,3 Ct. Каждый повтор описан. TCID 50 /мл = средняя инфекционная доза в тканевой культуре; WT = дикий тип; ∆S = шиповидный мутант S1/S2.
Анализ клеток в режиме реального времени продемонстрировал сопоставимую кинетику репликации для штаммов WT и ∆S SARS-CoV-2 ( рис. 4 ). Не наблюдалось существенной разницы в жизнеспособности клеток между WT и ∆S в любой момент времени. Через 48 ч после инфицирования жизнеспособность клеток WT и ∆S значительно отличалась от таковой при имитационной инфекции ( p < 0,05).
Рисунок 4. Способность к репликации SARS-CoV-2 WT и ∆S SARS-CoV-2, измеренная с помощью анализа клеток в реальном времени. Точки данных соответствуют площади под кривой анализа нормализованного клеточного индекса (электронный импеданс RTCA, установленный во время инокуляции) с 12-часовыми интервалами. Затем определяли жизнеспособность клеток путем нормализации относительно соответствующего клеточного контроля. WT = дикий тип; ∆S = S1/S2 шиповидный мутант.
- Обсуждение
Комбинация бромелаина и ацетилцистеина, BromAc, синергетически ингибировала инфекционность двух штаммов SARS-CoV-2, культивируемых на клетках Vero. Подтверждение белка и его молекулярные свойства зависят от его структурной и геометрической целостности, которая зависит как от пептидных связей, так и от дисульфидных мостиков. Ацетилцистеин, как хороший восстановитель, имеет тенденцию восстанавливать дисульфидные мостики и, следовательно, изменять молекулярные свойства большинства белков. Это свойство широко использовалось при разработке ряда методов лечения (хроническая обструктивная болезнь легких, аллергические заболевания дыхательных путей, муковисцидоз, псевдомиксома брюшины и др.) [ 20 , 23 , 24 , 25 , 26 , 27 ].]. Совсем недавно ацетилцистеин использовался при разработке методов лечения респираторных инфекций, таких как грипп и COVID-19 [ 28 , 29 , 30 ], где целостность шиповидного белка жизненно важна для инфекции [ 12 , 13 ]. Предполагаемый механизм действия может заключаться в разворачивании шиповидного гликопротеина и восстановлении его дисульфидных связей.
Спайковый белок SARS-CoV-2 является краеугольным камнем связывания вириона с клетками-хозяевами и, следовательно, представляет собой идеальную терапевтическую мишень. Прямое механическое воздействие на этот шиповидный белок представляет собой другую стратегию лечения по сравнению с большинством существующих противовирусных препаратов, которая предотвращает проникновение вируса в клетки-хозяева, а не воздействует на механизм репликации. BromAc действует как биохимический агент для разрушения сложных гликопротеинов. Мультипотентные ферментативные способности бромелаина, в которых преобладает способность разрушать гликозидные связи, с пользой дополняют сильную способность ацетилцистеина восстанавливать дисульфидные связи [ 17 ]. Анализ аминокислотной последовательности гликопротеина шипа SARS-CoV-2 выявил несколько предопределенных сайтов, где BromAc может действовать преимущественно, например, сайт S2', богатый дисульфидными связями [1].31 ], вместе с тремя другими дисульфидными связями в RBD [ 32 ]. Параллельно с этим роль гликозидного щита в покрытии шипа, который склонен к удалению BromAc, была выделена как элемент стабилизации конформационных переходов RBD, а также как механизм устойчивости к специфическому иммунному ответу [ 5 , 33 , 34 ]. ].
Клетки млекопитающих проявляют восстановительные функции на своей поверхности, которые способны расщеплять дисульфидные связи, и было доказано, что регуляция этого тиол-дисульфидного баланса влияет на интернализацию различных типов вирусов, включая SARS-CoV-2 [ 8 , 35 , 36 ]. , 37 , 38 ]. И ACE2, и шиповидные белки обладают дисульфидными связями. Когда все дисульфидные связи RBD белка шипа были восстановлены до тиолов, связывание рецептора ACE2 с белком шипа стало менее благоприятным [ 8 ]. Интересно, что уменьшение дисульфидных связей ACE2 также индуцировало уменьшение связывания [ 8]. Более того, в других сообщениях предполагалось, что бромелайн сам по себе может ингибировать инфекцию SARS-CoV-2 в клетках VeroE6 посредством действия на дисульфидные связи [ 39 , 40 ]. Таким образом, потеря инфекционности SARS-CoV-2, наблюдаемая после предварительной обработки BromAc, может быть связана с кумулятивным развертыванием белков шипа и оболочки со значительным снижением их дисульфидных связей под действием ацетилцистеина, продемонстрированным in vitro.
Интересно, что аналогичный эффект BromAc наблюдался как против дикого типа, так и против ∆S SARS-CoV-2. Основное различие в аминокислотных последовательностях между SARS-CoV-2 и предыдущим SARS-CoV заключается во включении сайта расщепления фурином между доменами S1 и S2 [ 41 ]. Это особое местонахождение спайкового белка и его роль в переносе хозяина и приспособленности вируса является предметом многочисленных споров [ 41 , 42 , 43 , 44 ].]. Следует отметить, что ∆S, который содержит мутацию в этом новом сайте расщепления S1/S2 и изменяет мотив расщепления, не проявляет явных различий в способности к репликации по сравнению со штаммом WT. Слегка повышенная чувствительность ∆S к обработке BromAc, таким образом, не является следствием смещения базовой репликации, но мутация, возможно, может быть связана с усилением механизма действия BromAc. Эти результаты, тем не менее, позволяют предположить, что при пороговой дозе BromAc потенциально может быть эффективен в отношении штаммов с мутантными шипами. Это может быть явным преимуществом BromAc по сравнению со специфическими иммунологическими механизмами спайк-специфической вакцинации [ 3 , 4 ].
На сегодняшний день были протестированы различные стратегии лечения, но ни одна молекула не продемонстрировала явного противовирусного эффекта. Кроме того, учитывая гетерогенный исход заболевания у пациентов с COVID-19, стратегия лечения должна сочетать несколько механизмов действия и быть адаптирована к стадии заболевания. Таким образом, перепрофилирование лечения остается идеальной стратегией против COVID-19, пока не будет достигнут достаточный охват вакцинацией во всем мире [ 45 , 46 ]. В частности, разработка раннего назального лечения, направленного на снижение контагиозности пациента и предотвращение прогрессирования тяжелых легочных форм, имеет веское обоснование. Хоу и др. продемонстрировали, что первым очагом инфекции является слизистая оболочка носоглотки с вторичным перемещением в легкие путем аспирации.47 ]. Действительно, картина инфекционности клеток дыхательных путей соответствовала экспрессии рецептора ACE2, снижаясь от верхних дыхательных путей к альвеолярной ткани. Соотношение для ACE2 было в пять раз выше в носу, чем в дистальных отделах дыхательных путей [ 40 ]. В лабораторных условиях были протестированы и другие методы лечения в качестве назального антисептика, такие как повидон-йод, который показал активность против SARS-CoV-2 [ 48 ].]. В настоящем исследовании мы показали in vitro терапевтический потенциал BromAc против SARS-CoV-2 с пороговой эффективной дозой 100 мкг/20 мг/мл. Поскольку на сегодняшний день модели безопасности дыхательных путей у двух видов животных не показали токсичности (неопубликованные данные), цель состоит в том, чтобы протестировать назальное введение препарата в ходе I фазы клинических испытаний (ACTRN12620000788976). Такое лечение может помочь смягчить легкие инфекции и предотвратить заражение лиц, регулярно контактирующих с вирусом, таких как медицинские работники.
Хотя наши результаты обнадеживают, есть ряд моментов, которые следует учитывать в отношении этой демонстрации. А именно, условия in vitro фиксированы и могут отличаться от условий in vivo. На любую ферментативную реакцию влияет рН среды, и тем более, когда речь идет о окислительно-восстановительных реакциях, таких как восстановление дисульфидных связей [ 9 ]. В физиологических условиях pH слизистой оболочки носа составляет от 5,5 до 6,5 и повышается при рините до 7,2–8,3 [ 49 ]. Пожилой возраст, часто встречающийся при симптоматических инфекциях SARS-CoV-2, также вызывает повышение pH слизистой оболочки носа [ 49 ].]. Такой диапазон вариаций, зависящий от модификаций, обычно вызываемых вирусной инфекцией, может поставить под вопрос эффективность нашей стратегии лечения. Дальнейшие эксперименты in vitro для проверки различных условий pH продолжаются, но в конечном итоге только клинические исследования смогут оценить этот момент. Наши эксперименты проводились на клеточной линии почек обезьян, которая, как известно, обладает высокой восприимчивостью к инфекционности SARS-CoV-2. С учетом вышеизложенной гипотезы о нарушении тиол-дисульфидного баланса лизиса S-белка эффективность BromAc в отношении SARS-CoV-2 не должна зависеть от структуры мембранных протеаз. Воспроизведение этого экспериментального протокола с клеточной линией легочного эпителия Calu-3 человека (ATCC ® HTB-55™) позволит решить эти вопросы, поскольку проникновение вируса зависит от TMPRSS2 и pH-независимо, как в эпителии дыхательных путей, в то время как проникновение вируса в клетки Vero зависит от катепсина L и, следовательно, зависит от pH [ 50 ] .
В целом, результаты, полученные в ходе настоящего исследования в сочетании с дополнительными исследованиями свойств BromAc и характеристик SARS-CoV-2, свидетельствуют о том, что BromAc может быть превращен в эффективное терапевтическое средство против SARS-CoV-2.
- Выводы
В настоящее время не существует подходящего терапевтического лечения раннего SARS-CoV-2, направленного на предотвращение прогрессирования заболевания. BromAc находится в стадии клинической разработки авторами для лечения муцинозного рака из-за его способности изменять сложные структуры гликопротеинов. Был изучен потенциал BromAc в отношении белков шипа и оболочки SARS-CoV-2, стабилизированных дисульфидными связями, и было обнаружено, что он вызывает разворачивание рекомбинантных белков шипа и оболочки за счет уменьшения дисульфидных стабилизирующих мостиков. BromAc также продемонстрировал ингибирующее действие на мутантный штамм SARS-CoV-2 дикого типа и шиповидный за счет инактивации его способности к репликации in vitro. Следовательно, BromAc может быть эффективным терапевтическим средством для ранней инфекции SARS-CoV-2, несмотря на мутации, и даже иметь потенциал в качестве профилактического средства у людей с высоким риском заражения.
Вклад автора
Концептуализация, JA, KP, SJV и DLM; методология, JA, GQ, KP, SB и AHM; валидация, JA, GQ, KP, VK, SB и AHM; расследование, JA, GQ, KP, VK, SB и AHM; написание - подготовка исходного проекта, GQ, KP, VK, AHM, EF и SJV; супервизия, DLM и EF; администрирование проекта, SJV; приобретение финансирования, SJV и DLM Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование
Это исследование частично финансируется Mucpharm Pty Ltd., Австралия.
Заявление о доступности данных
Препринт этой рукописи был заархивирован на сайте www.biorxiv.org (по состоянию на 31 января 2021 г.) в связи с чрезвычайной ситуацией, связанной с COVID-19.
Конфликт интересов
Дэвид Л. Моррис является соавтором и правопреемником лицензии на это исследование и директором дочерней спонсорской компании Mucpharm Pty Ltd. Джавед Ахтер, Кришна Пиллаи и Ахмед Меккави являются сотрудниками Mucpharm Pty Ltd. частично используется Mucpharm для разработки рака и поддерживается стипендией австралийского правительства по исследовательской программе обучения. Ваан Кепенекян благодарит Фонд Nuovo Soldati за его помощь и частично спонсировал стипендию Mucpharm Pty Ltd.
использованная литература
- Ресурсный центр по коронавирусу Университета Джона Хопкинса. Информационная панель COVID-19 Центра системных наук и инженерии (CSSE) Университета Джона Хопкинса (JHU). Доступно в Интернете: https://coronavirus.jhu.edu/map.html (по состоянию на 7 февраля 2021 г.).
- Песня, Ю.; Чжан, М .; Инь, Л .; Ван, К.; Чжоу, Ю .; Чжоу, М .; Лу, Ю. Лечение COVID-19: близко к излечению? – быстрый обзор фармакотерапии нового коронавируса. Дж. Антимикроб. Agents 2020 , 56 , 106080. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Чжу, ФК; Гуань, XH; Ли, ЮХ; Хуанг, JY; Цзян, Т .; Хоу, Л.Х.; Ли, JX; Ян, Б.Ф.; Ван, Л.; Ван, WJ; и другие. Иммуногенность и безопасность рекомбинантной вакцины против COVID-19 с вектором аденовируса типа 5 у здоровых взрослых в возрасте 18 лет и старше: рандомизированное двойное слепое плацебо-контролируемое исследование фазы 2. Ланцет 2020 , 396 , 479–488. [ Академия Google ] [ Перекрестная ссылка ]
- Фолегатти, премьер-министр; Эвер, К.Дж.; Алей, ПК; Ангус, Б.; Беккер, С.; Белий-Раммерсторфер, С.; Беллами, Д.; Биби, С .; Биттай, М .; Клаттербак, EA; и другие. Безопасность и иммуногенность вакцины ChAdOx1 nCoV-19 против SARS-CoV-2: предварительный отчет фазы 1/2, одиночного слепого, рандомизированного контролируемого исследования. Ланцет 2020 , 396 , 467–478. [ Академия Google ] [ Перекрестная ссылка ]
- Кай, Ю .; Чжан, Дж.; Сяо, Т .; Пэн, Х .; Стерлинг, С.М.; Уолш, Р. М., младший; Роусон, С.; Ритс-Воллох, С.; Чен, Б. Различные конформационные состояния спайкового белка SARS-CoV-2. Наука 2020 , 369 , 1586–1592. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Кутар, Б.; Валле, К.; де Ламбальри, X .; Канард, Б.; Сейда, Н.Г.; Декроли, Э. Гликопротеин спайка нового коронавируса 2019-nCoV содержит фуриноподобный сайт расщепления, отсутствующий в CoV той же клады. Противовирусный рез. 2020 , 176 , 104742. [Академия Google ] [ CrossRef ]
- Ванкадари, Н .; Wilce, JA Emerging WuHan (COVID-19) коронавирус: гликановый щит и предсказание структуры шиповидного гликопротеина и его взаимодействия с CD26 человека. микробы заражают. 2020 , 9 , 601–604. [ Академия Google ] [ Перекрестная ссылка ]
- Шляпа это.; Бхаттачарья, С. Влияние тиол-дисульфидного баланса на связывание шиповидного белка Covid-19 с рецептором ангиотензинпревращающего фермента 2. САУ Омега 2020 , 5 , 16292–16298. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Лавиллетт, Д.; Барбуш, Р.; Яо, Ю .; Бозон, Б.; Коссет, Флорида; Джонс, И. М.; Fenouillet, E. Значительная нечувствительность к окислительно-восстановительному потенциалу функций шиповидного гликопротеина SARS-CoV: сравнение с оболочкой ВИЧ. биол. хим. 2006 , 281 , 9200–9204. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Мэтис, Л.; Бальзарини, Дж. Роль клеточных оксидоредуктаз в проникновении вируса и окислительном стрессе, связанном с вирусной инфекцией: потенциальное терапевтическое применение. мнение тер. Цели на 2016 г., 20 , 123–143. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Обертка, Д.; Ван, Н.; Корбетт, Канзас; Голдсмит, Дж. А.; Се, К.-Л.; Абиона, О .; Грэм, бакалавр наук; Маклеллан, Дж. С. Крио-ЭМ-структура шипа 2019-nCoV в конформации до слияния. Наука 2020 , 367 , 1260–1263. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Морейра, РА; Гусман, Х.В.; Бупати, С.; Бейкер, Дж. Л.; Пома, А. Б. Количественное определение механической стабильности шиповидного белка нового коронавируса. Nanoscale 2020 , 12 , 16409–16413. [ Академия Google ] [ Перекрестная ссылка ]
- Морейра, РА; Гусман, Х.В.; Бупати, С.; Бейкер, Дж. Л.; Пома, А.Б. Характеристика структурных и энергетических различий между конформациями шиповидного белка SARS-CoV-2. Материалы 2020 , 13 , 5362. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Амини, А .; Масуми-Могхаддам, С.; Моррис, Д.Л. Применение бромелаина и N-ацетилцистеина в лечении перитонеальной диссеминации желудочно-кишечных муцинпродуцирующих злокачественных новообразований ; Springer: New York, NY, USA, 2016. [ Google Scholar ]
- Шлегель, А .; Шаллер, Дж.; Дженч, П.; Кемпф, К. Фрагментация ядра белка лесного вируса Семлики: его возможная роль в разборке нуклеокапсида. 1993 , 13 , 333–347 . [ Академия Google ] [ Перекрестная ссылка ]
- Грейг, А.С.; Bouillant, AM Связывающие эффекты конканавалина А на коронавирус. Дж. Комп. Мед. 1977 , 41 , 122–126. [ Академия Google ]
- Пиллаи, К.; Ахтер, Дж.; Чуа, ТК; Моррис, Д.Л. Препарат для лизиса in situ муцина, секретируемого при псевдомиксоме брюшины. Дж. Рак 2014 , 134 , 478–486. [ Академия Google ] [ Перекрестная ссылка ]
- Шуман, Д.; Филдинг, до н.э. Белок оболочки коронавируса: современные знания. J. 2019 , 16 , 69. [ Google Scholar ] [ CrossRef ][ Green Version ]
- Пиллаи, К.; Ахтер, Дж.; Моррис, Д.Л. Оценка нового муколитического раствора для растворения слизи при псевдомиксоме брюшины: исследование ex vivo и in vitro. Плевра Перитонеум 2017 , 2 , 111–117. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Валле, С.Дж.; Ахтер, Дж.; Меккави, А.Х.; Лод, С .; Пиллаи, К.; Бадар, С .; Гленн, Д.; Мощность, М.; Лиау, В .; Моррис, Д.Л. Новое лечение бромелаином и ацетилцистеином (BromAc) у пациентов с перитонеальными муцинозными опухолями: первая фаза исследования на людях. Дж. Сур. Онкол. 2021 , 47 , 115–122. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Пиллаи, К.; Меккави, А.Х.; Ахтер, Дж.; Бадар, С .; Донг, Л.; Лю, А.И.; Моррис, Д.Л. Повышение эффективности химиотерапевтических средств в сочетании с бромелаином и N-ацетилцистеином — исследование in vitro с раковыми клетками поджелудочной железы и печени. Дж. Пер. Рез. 2020 , 12 , 7404–7419. [ Академия Google ]
- Айер, Канзас; Клее В.А. Прямое спектрофотометрическое измерение скорости восстановления дисульфидных связей. Реакционная способность дисульфидных связей бычьего -лактальбумина. биол. хим. 1973 , 248 , 707–710. [ Академия Google ]
- Чжан, В.; Ю, Ю .; Май.; Ван, Т. N-ацетилцистеин улучшает окислительный стресс и воспалительную реакцию у пациентов с внебольничной пневмонией: рандомизированное контролируемое исследование. Медицина 2018 , 97 , 45. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Морган, LE; Джарамилло, AM; Шеной, СК; Рацлавская, Д.; Эмезиенна, Н.А.; Ричардсон, В.Л.; Хара, Н.; Тяжелее, AQ; НиДелл, Дж. К.; Hennessy, CE Дисульфидное разрушение устраняет дисфункцию слизи при аллергических заболеваниях дыхательных путей. коммун. 2021 , 12 , 1–9. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Кальзетта, Л.; Рольяни, П.; Фаччоло, Ф.; Ринальди, Б.; Каззола, М .; Матера, MG N-ацетилцистеин защищает бронхи человека, модулируя высвобождение нейрокинина А в ex vivo модели обострения ХОБЛ. Биомед Фарм. 2018 , 103 , 1–8. [ Академия Google ] [ Перекрестная ссылка ]
- Каззола, М .; Кальзетта, Л.; Фаччоло, Ф.; Рольяни, П.; Матера, М.Г. Фармакологическое исследование антиоксидантной и противовоспалительной активности N-ацетилцистеина в модели обострения ХОБЛ ex vivo. Рез. 2017 , 18 , 26. [ Академия Google ] [ CrossRef ] [ PubMed ]
- Сук, Дж. С.; Бойлан, Нью-Джерси; Трехан, К .; Тан, Британская Колумбия; Шнайдер, CS; Лин, Дж.-М.Г.; Бойл, член парламента; Цейтлин, PL; Лай, СК; Cooper, MJ N-ацетилцистеин усиливает проникновение муковисцидоза в мокроту и перенос генов в дыхательные пути с помощью сильно уплотненных наночастиц ДНК. тер. 2011 , 19 , 1981–1989. [ Академия Google ] [ Перекрестная ссылка ]
- Сухайл, С .; Заджак, Дж.; Фоссум, К.; Лоуотер, Х .; Маккракен, К.; Северсон, Н.; Латч, Б.; Наркевич-Йодко, А.; Джонсон, Б.; Либау, Дж. Роль окислительного стресса в инфекции SARS-CoV (SARS) и SARS-CoV-2 (COVID-19): обзор. Протеин Дж. 2020 , 39 , 1–13. [ Академия Google ] [ Перекрестная ссылка ]
- Де Флора, С.; Баланский Р.; Ла Маэстра, С. Обоснование использования N-ацетилцистеина как для профилактики, так и для адъювантной терапии COVID-19. FASEB J. 2020 , 34 , 13185–13193. [ Академия Google ] [ Перекрестная ссылка ]
- Герреро, Калифорния; Акоста О. Воспалительный и окислительный стресс при ротавирусной инфекции. Мир Дж. Вирол. 2016 , 5 , 38. [ Академия Google ] [ CrossRef ] [ PubMed ]
- Стены, кондиционер; Парк, Ю.Дж.; Торторичи, Массачусетс; Уолл, А .; Макгуайр, AT; Вислер, Д. Структура, функция и антигенность гликопротеина шипа SARS-CoV-2. Ячейка 2020 , 181 , 281–292. е6. [ Академия Google ] [ Перекрестная ссылка ]
- Ли, В .; Чжан, К.; Суй, Дж.; Кун, Дж. Х.; Мур, МДж; Луо, С .; Вонг, СК; Хуанг, IC; Сюй, К .; Васильева Н.; и другие. Рецепторные и вирусные детерминанты адаптации SARS-коронавируса к ACE2 человека. EMBO J. 2005 , 24 , 1634–1643. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Green Version ]
- Ватанабэ, Ю.; Аллен, JD; Обертка, Д.; Маклеллан, Дж. С.; Криспин, М. Сайт-специфический анализ гликанов шипа SARS-CoV-2. Наука 2020 , 369 , 330–333. [ Академия Google ] [ Перекрестная ссылка ]
- Казалино, Л.; Гаиб, З .; Голдсмит, Дж. А.; Хьорт, CK; Доммер, AC; Харбисон, AM; Фогарти, Калифорния; Баррос, EP; Тейлор, Британская Колумбия; Маклеллан, Дж. С. Помимо экранирования: роль гликанов в спайковом белке SARS-CoV-2. Цент ACS. науч. 2020 , 6 , 1722–1734. [ Академия Google ] [ Перекрестная ссылка ]
- Райзер, Х .; Леви, Э.М.; Мандель, Р.; DiSciullo, GJ Ингибирование инфекции вируса иммунодефицита человека агентами, которые препятствуют обмену тиол-дисульфид при взаимодействии вирус-рецептор. Натл. акад. науч. США 1994 , 91 , 4559–4563. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Green Version ]
- Кеннеди С.И. Влияние ферментов на структурно-биологические свойства лесного вируса Семлики. Генерал Вирол. 1974 , 23 , 129–143. [ Академия Google ] [ Перекрестная ссылка ]
- Шлегель, А .; Омар, А .; Дженч, П.; Морелл, А .; Кемпф, К. Белки оболочки лесного вируса Семлики функционируют как протонные каналы. 1991 , 11 , 243–255 . [ Академия Google ] [ Перекрестная ссылка ]
- Compans, RW Расположение гликопротеина в мембране вируса Синдбис. Новая биол. 1971 , 229 , 114–116. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Сагар, С .; Ратинавель, Аляска; Лутц, ЗЕ; Страбле, ЛР; Хурана, С .; Шнаубельт, А.Т.; Мишра, Северная Каролина; Гуда, К.; Палермо, Нью-Йорк; Бродхерст, MJ; и другие. Бромелайн ингибирует инфекцию SARS-CoV-2, воздействуя на ACE-2, TMPRSS2 и шиповидный белок. Перевод Мед. 2021 , 11 , 2. [ Google Scholar ] [ CrossRef ]
- Корбер, Б.; Фишер, В.М.; Гнанакаран, С.; Юн, Х .; Тайлер, Дж.; Абфальтерер, В.; Хенгартнер, Н.; Георгий, Э.Э.; Бхаттачарья, Т .; Фоли, Б. Отслеживание изменений в шипе SARS-CoV-2: доказательства того, что D614G повышает инфекционность вируса COVID-19. Ячейка 2020 , 182 , 812–827. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Чжоу, Х .; Чен, X .; Хижина.; Ли, Дж.; Песня, Х .; Лю, Ю.; Ван, П.; Лю, Д.; Ян, Дж .; Холмс, ЕС; и другие. Новый коронавирус летучих мышей, тесно связанный с SARS-CoV-2, содержит естественные вставки в сайте расщепления S1/S2 шиповидного белка. биол. 2020 , 30 , 2196–2203. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Джеймс, Дж. А.; Милле, Дж. К.; Уиттакер, Г.Р. Протеолитическое расщепление спайкового белка SARS-CoV-2 и роль нового сайта S1/S2. iScience 2020 , 23 , 101212. [ Академия Google ]
- Лау, С.Ю.; Ван, П.; Мок, ЧБ; Чжан, А.Дж.; Чу, Х .; Ли, переменный ток; Дэн, С .; Чен, П.; Чан, К. Х.; Песня, В .; и другие. Аттенуированные варианты SARS-CoV-2 с делециями на стыке S1/S2. Emerg Microbes Infect 2020 , 9 , 837–842. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Хоффманн, М .; Кляйне-Вебер, Х .; Полманн, С. Сайт многоосновного расщепления в шиповидном белке SARS-CoV-2 необходим для инфицирования клеток легких человека. Ячейка 2020 , 78 , 779–784. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Уолш, Э.Э.; Френк, Р.В., младший; Фолси, Арканзас; Китчин, Н .; Абсалон, Дж.; Гуртман, А .; Локхарт, С.; Нейзил, К.; Маллиган, М.Дж.; Бейли, Р.; и другие. Безопасность и иммуногенность двух вакцин-кандидатов на основе РНК Covid-19. англ. Дж. Мед. 2020 , 383 , 2439–2450. [ Академия Google ] [ Перекрестная ссылка ]
- Андерсен, частный детектив; Яневский, А .; Лисванд, Х .; Виткаускене, А .; Оксеныч, В.; Бьорас, М .; Теллинг, К.; Луцарь, И.; Думпис, У .; Ирие, Ю.; и другие. Открытие и разработка безопасных для человека противовирусных препаратов широкого спектра действия. Дж. Заразить. Дис. 2020 , 93 , 268–276. [ Академия Google ] [ Перекрестная ссылка ]
- Хоу, Ю.Дж.; Окуда, К .; Эдвардс, CE; Мартинес, доктор медицины; Асакура, Т .; Диннон, KH, 3-й; Като, Т .; Ли, RE; Юнт, Б.Л.; Масценик, ТМ; и другие. Обратная генетика SARS-CoV-2 выявила переменный градиент инфекции в дыхательных путях. Cell 2020 , 182 , 429–446.e14. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Франк, С .; Браун, С.М.; Каприотти, Дж. А.; Вестовер, Дж. Б.; Пеллетье, Дж. С.; Тессема, Б. Эффективность in vitro повидон-йодного назального антисептика для быстрой инактивации SARS-CoV-2. JAMA Отоларингол. Хирургия головы и шеи. 2020 , 146 , 1054–1058. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Англия, Р. Дж.; Гомер, Джей Джей; Рыцарь, ЛК; Элл, С.Р. Назальное измерение pH: надежный и воспроизводимый параметр. Отоларингол. Союзн. наук. 1999 , 24 , 67–68. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Хоффманн, М .; Мосбауэр, К.; Хофманн-Винклер, Х .; Каул, А .; Кляйне-Вебер, Х .; Крюгер, Н.; Гассен, Северная Каролина; Мюллер, Массачусетс; Дростен, К.; Pohlmann, S. Хлорохин не ингибирует заражение клеток легких человека SARS-CoV-2. Природа 2020 , 585 , 588–590. [ Академия Google ] [ Перекрестная ссылка ]
Примечание издателя: MDPI остается нейтральным в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности. |
© 2021 авторами. Лицензиат MDPI, Базель, Швейцария. Эта статья находится в открытом доступе и распространяется на условиях лицензии Creative Commons Attribution (CC BY) ( http://creativecommons.org/licenses/by/4.0/ ).
Делитесь и цитируйте
MDPI и стиль ACS
Ахтер, Дж.; Керомес, Г.; Пиллаи, К.; Кепенекян, В .; Бадар, С .; Меккави, А.Х.; Фроберт, Э.; Валле, С.Дж.; Моррис, Д.Л. Комбинация бромелаина и ацетилцистеина (BromAc) синергетически инактивирует SARS-CoV-2. Вирусы 2021 , 13 , 425. https://doi.org/10.3390/v13030425
Стиль АМА
Ахтер Дж., Керомес Г., Пиллаи К., Кепенекян В., Бадар С., Меккави А.Х., Фроберт Э., Валле С.Дж., Моррис Д.Л. Комбинация бромелаина и ацетилцистеина (BromAc) синергетически инактивирует SARS-CoV-2. Вирусы . 2021; 13(3):425. https://doi.org/10.3390/v13030425
Чикаго/Турабиан Стиль
Ахтер, Джавед, Грегори Керомес, Кришна Пиллаи, Ваан Кепенекян, Самина Бадар, Ахмед Х. Меккави, Эмили Фроберт, Сара Дж. Валле и Дэвид Л. Моррис. 2021. «Комбинация бромелаина и ацетилцистеина (BromAc) синергетически инактивирует вирусы SARS-CoV-2» 13, вып. 3: 425. https://doi.org/10.3390/v13030425

Комментарии
Люди «кажутся» просто «сногсшибательными» без видимой причины.